Laporan Praktikum Sintesis Senyawa Kompleks Cis dan Trans Kalium Diakuodioksalato Kromat (III)
Percobaan berjudul Sintesis Senyawa Kompleks Cis dan Trans-Kalium Dioksalatodiakuo Kromat (III) bertujuan untuk mensintesis senyawa kompleks cis dan trans dari garam kompleks kalium dioksalatodiakuo kromat (III) dan untuk mempelajari sifat-sifat isomer cis dan trans dari garam kompleks kalium dioksalatodiakuo kromat (III).
A. Tujuan
- Mensintesis senyawa kompleks cis dan trans dari garam kompleks kalium diakuodioksalato kromat (III)
- Mempelajari sifat-sifat isomer cis dan trans dari garam kompleks kalium diakuodioksalato kromat (III)
B. Dasar Teori
1. Senyawa Kompleks
Senyawa kompleks merupakan senyawa yang tersusun dari suatu ion logam pusat dengan satu atau lebih ligan yang menyumbangkan pasangan elektron bebasnya kepada in logam pusat. Donasi pasangan-pasangan elektron bebasnya kepada ion logam pusat menghasilkan ikatan kovalen koordinasi sehingga senyawa kompleks juga disebut senyawa koordinasi (Cotton dan Wilkinson, 1984).
Semua senyawa kompleks atau senyawa koordinasi adalah senyawa yang terjadi karena adanya ikatan kovalen koordinasi antara logam transisi dengan satu atau lebih ligan (Sukardjo, 1992).
Senyawa kompleks sangat berhubungan dengan asam dan basa lewis dimana asam lewis adalah senyawa yang dapat bertindak sebagai penerima pasangan bebas sedangkan basa lewis adalah senyawa yang bertindak sebagai penyumbang pasangan elektron (Shriver, 1940).
2. Ligan
Senyawa ion logam yang berkoordinasi dengan ligan disebut dengan senyawa kompleks. Sebagian besar ligan merupakan zat netral atau anionic tetapi kation seperti kation tropilium juga dikenal sebagai ligan. Ligan netral seperti amonia (NH3) atau karbon monoksida (CO2) dalam keadaan bebas merupakan molekul yang stabil, sementara ligan anionic seperti Cl- atau C5H5- distabilkan hanya jika dikoordinasikan ke atom logam pusat. Ligan representatif menurut unsur yang mengikatnya. Ligan umum atau dengan rumus kimia rumit diungkapkan dengan singkatanyya (Saito, 1996).
Ligan seperti I-, NH3, CN- hanya memiliki satu atom donor pasangan elektron dan disebut monodentate. Ligan yang mempunyai atom donor lebih dari satu disebut multidentate, pentadentate, dan seterusnya bila mempunyai atom donor pasangan elektron sebanyak 3, 4, 5, 6. Contoh ligan bidentat adalah etilena diamin yang memiliki dua atom donor yaitu kedua atom N dan 8-hidroksikuinolin (oksin). Sedangkan ligan polidentat contohnya adalah EDTA yang memiliki enam buah atom donor pasangan elektron yaitu melalui kedua atom N dan keempat atom O (dari OH) (Harjadi, 1990).
3. Isomer (Cis dan Trans)
Isomer adalah dua atau lebih spesies yang mempunyai komposisi (rumus molekul) sama tetapi mempunyai struktur dan sifat yang berbeda. Terdapat beberapa jenis isomer yang terjadi pada ion kompleks dan senyawa koordinasi. Stereoisomer-stereoisomer memiliki kesamaan pada tingkat ikatan tetapi berbeda dalam susunan geometri atau penyusunan ligan dalam ruang. Dari lima jenis isomer, tiga yang pertama menunjukkan isomer struktur dan dua sisanya stereoisomer (Achnadi, 1987).
Isomer geometri adalah isomer yang disebabkan oleh perbedaan letak atom atau gugus di dalam ruang. Isomer geometri sering disebut juga dengan isomer cis-trans. Isomer ini tidak terdapat paada kompleks dengan struktur linear, trigonal planar, atau tetrahedral, tetapi umumnya terdapat pada kompleks planar segiempat dan octahedral. Isomer geometri cis dan trans adalah jenis isomer yang disebabkan oleh bentuk molekul yang kaku dan hanya dalam senyawa golongan alkena dan siklis. Atom atau gugus yang hanya diikat oleh ikatan sigma dapat berputar sehingga bentuk keseluruhan molekul selalu berubah. Tetapi gugus yang diikat oleh ikatan ganda tidak dapat berputar mengelilingi ikatan ganda tersebut (Sumo, 1992).
Bila pada suatu reaksi terbentuk campuran isomer cis-trans maka untuk memperoleh masing-masing isomer perlu diadakan pemisahan. Pemisahan isomer ini dapat dilakukan dengan cara kristalisasi bertingkat ion exchange atau cara-cara fisika lainnya. Cis dan trans dapat dibedakan dengan mereaksikan zat tersebut dengan asam oksalat. Pada senyawa cis dapat diikat satu gugus oksalat sedangkan pada senyawa trans dapat diikat dua gugus oksalat (Sukardjo, 1992).
4. Kristalisasi
Kristalisasi adalah metode pemisahan dengan cara pembentukan kristal sehingga campuran dapat dipisahkan. Suatu zat gas dan cair dapat didinginkan atau memadat serta membentuk kristal karena mengalami proses kristalisasi. Kristal-kristal juga akan terbentuk dari suatu larutan yang akan dijenuhkan dengan pelarut tertentu. Semakin banyak kristalnya, maka semakin baik karena semakin kecil kemungkinan tercemar oleh kotoran (Arsyad, 2001).
Adapun proses kristalisasi dapat dilakukan dengan cara sebagai berikut:
a. Kristalisasi dengan Penguapan
Kelarutan suatu bahan yang berkurang sedikit demi sedikit dengan menurunnya suhu. Kondisi lewat jenuhnya dapat dipakai dengan penguapan sebagai pelarut.
b. Kristalisasi dengan Pendinginan
Kelarutan suatu bahan yang berkurang drastis dengan menurunnya suhu. Kondisi lewat jenuh dicapai dengan pendinginan larutan panas yang jenuh. Untuk mengkristalisasi dari lelehan dapat juga dilakukan (Cahyono, 1991).
5. Efek Trans
Reaksi penggantian ligan dalam kompleks bujur sangkar dan octahedral melibatkan aspek stereokimia terutama adanya efek trans. Secara sterik terdapat dua kemungkinan dua produk reaksi dengan orientasi cis dan trans sangat beragam terhadap ligan L. perbandingan relatif produk cis dan trans sangat beragam terhadap ligan L.
Suatu deret ligan telah disusun berdasarkan kemampuannya mensubstitusi dalam posisi trans terhadapnya. Fenomena tersebut dikenal dengan efek trans. Urutan pengaruh trans yang semakin naik untuk reaksi substitusi pada pembentukan kompleks Pt (II) adalah:
CO, CN, C2H4 > PR3, NO > CH3-, SC(NH2)2 > C6H5-, NO2-, I-, SCN > Br- > Cl- > NH3, py, RNH2, F > OH- > H2O (Day dan Selbin, 1993).
C. Alat dan Bahan
Alat-alat yang digunakan pada percobaan ini adalah gelas beaker 250 mL, gelas beaker 100 mL, gelas beaker 50 mL, gelas ukur 25 mL, gelas ukur 5 mL, pipet tetes, corong gelas, gelas arloji kecil, gelas arloji besar, cawan penguapan, sendok sungu, pengaduk kaca, pompa vakum, kertas saring, pinset, spatula, magnetic stirrer, hot plate, neraca analitik, toples, label, dan botol akuades.
Bahan-bahan yang digunakan pada percobaan ini adalah larutan HNO3 0,01 M, larutan K2Cr2O7, asam oksalat, etanol 98%, es batu, dan akuades
D. Cara Kerja
1. Pembuatan isomer trans-kalium diakuodioksalato kromat (III)
Sebanyak 3 gram asam oksalat dihidrat di larutkan dengan 1 gram kalium dikromat dan 5 mL akuades. Kemudian dibiarkan menguap pada suhu kamar sampai tinggal sepertiganya. Lalu disaring dan dicuci dengan akuades dingin dan etanol.
2. Pembuatan isomer cis-kalium diakuodioksalato kromat (III)
sebanyak 1 gram kalium dikromat dicampurkan dengan 3 gram asam oksalat dihidrat. Kemudian ditetesi akuades dan ditutup dengan gelas arloji. Selanjutnya ditambahkan 5 mL etanol dan diaduk. Dekantir dan ditambahkan etanol baru. Kemudian disaring dan dikeringkan.
3. Uji Kemurnian Kristal
Kristal senyawa kompleks ditempatkan pada kertas saring dan ditambahkan larutan amonia encer.
E. Data Hasil Pengamatan
1. Pembuatan isomer trans-kalium diakuodioksalato kromat (III)
|
No. |
Cara Kerja |
Pengamatan |
|
1. |
Asam oksalat dilarutkan, ditambahkan larutan kalium dikromat dan akuades 5 mL |
Massa asam oksalat = 3,0575 gram Massa kalium dikromat = 1,0448 gram Warna menjadi kuning, hijau, coklat, lalu hitam |
|
2. |
Gelas beaker ditutup dengan gelas arloji |
Warna menjadi coklat kehitaman |
|
3. |
Uapkan hingga separuh |
Berwarna hitam |
|
4. |
Biarkan menguap dengan sendirinya hingga tinggal sepertiga |
Larutan berwarna hitam |
|
5. |
Disaring kemudian dicuci dengan akuades dingin dan etanol |
Massa isomer trans = 0,0104 gram Rendemen = 0,34% |
2. Pembuatan isomer cis-kalium diakuodioksalato kromat (III)
|
No. |
Cara Kerja |
Pengamatan |
|
1. |
Kalium dikromat dicampurkan dengan asam oksalat dihidrat |
Massa kalium dikromat = 1,0026 gram Massa asam oksalat = 3,0670 gram |
|
2. |
Setelah akuades diteteskan ditutup dengan gelas arloji |
Berubah warna menjadi hitam dan bereaksi, gelembung yang menyebar dengan cepat dan warnanya hitam |
|
3. |
Ditambahkan 5 mL etanol ditambahkan dan diaduk |
Terdapat endapan hitam |
|
4. |
Dekantir dan ditambahkan etanol baru |
- |
|
5. |
Disaring dan dikeringkan |
Massa isomer trans = 1,8667 gram Rendemen = 61,6% |
3. Uji Kemurnian Kristal
- Isomer cis: hijau menyebar
- Isomer trans: cokelat tidak menyebar
F. Pembahasan
Percobaan yang dilakukan berjudul Sintesis Senyawa Kompleks Cis dan Trans-Kalium Dioksalatodiakuo Kromat (III). Tujuan dari percobaan ini adalah untuk mensintesis senyawa kompleks cis dan trans dari garam kompleks kalium dioksalatodiakuo kromat (III) dan untuk mempelajari sifat-sifat isomer cis dan trans dari garam kompleks kalium dioksalatodiakuo kromat (III).
Prinsip kerja dari percobaan ini adalah kristalisasi penguapan berdasarkan kelarutan suatu bahan yang berkurang sedikit demi sedikit dengan menurunnya suhu sehingga menghasilkan senyawa kompleks cis dan trans kalium dioksalatodiakuo kromat (III). Isomer geometri cis dan trans merupakan jenis isomer yang disebabkan oleh molekul yang kaku dan hanya dalam senyawa golongan alkena dan siklis. Atom atau gugus yang hanya diikat oleh ikatan sigma dapat berputar dapat berputar sehingga bentuk molekul selalu berubah. Tetapi gugus yang diikat oleh ikatan ganda tidak dapat berputar mengelilingi ikatan ganda tersebut.
Pembuatan isomer trans-kalium dioksalatodiakuo kromat (III) dilakukan dengan melarutkan asam oksalat untuk menguraikan senyawa menjadi ion-ionnya yang kemudian dicampurkan. Pelarutan tersebut dilakukan untuk menguraikan senyawa menjadi ion-ionnya yang kemudian dicampurkan dan terbentuk senyawa kompleks kalium dioksalatodiakuo kromat (III) yang ditandai dengan perubahan warna menjadi kuning-hijau-coklat lalu kehitaman. Reaksi yang terjadi saat pelarutan sebagai berikut:
Reaksi yang terjadi saat pencampuran sebagai berikut:
Campuran kemudian diuapkan hingga sepertiga, kemudian dibiarkan menguap pada temperatur kamar dan dihasilkan endapan yang berwarna hitam dengan sedikit larutan yang berwarna hitam. Endapan yang dihasilkan disaring dan dicuci menggunakan akuades dingin untuk menghilangkan pengotor yang ada dalam endapan. Pencucian dilanjutkan menggunakan etanol untuk menghilangkan pengotor yang masih terdapat dalam endapan dan tidak hilang saat dicuci menggunakan akuades dingin. Saat penyaringan menggunakan penyaring buchner, larutan ikut tersaring seluruhnya sehingga sedikit terdapat endapan isomer trans-kalium diokasalatodiakuo kromat (III). Hal ini terjadi karena reaksinya tidak berlangsung secara sempurna sehingga diperoleh massa isomer trans-kalium dioksalatodiakuo kromat (III) sebesar 0,0104 gram. Rendemen yang diperoleh sebesar 0,34%.
Pembuatan isomer cis-kalium dioksalatodiakuo kromat (III) dilakukan dengan pencampuran kalium dikromat dengan asam oksalat dihidrat. Senyawa kompleks kalium dioksalatodiakuo kromat (III) terbentuk saat campuran ditetesi dengan setetes akuades yang ditandai dengan perubahan warna menjadi hitam dan gelembung yang menyebar dengan cepat pada permukaan campuran. Reaksi yang terjadi saat campuran ditetesi dengan akuades adalah sebagai berikut:
Saat ditambahkan etanol terbentuklah endapan hitam. Etanol berfungsi untuk menghilangkan pengotor dan ditambahkan etanol baru untuk mencuci endapan. Pencucian dilakukan untuk menghilangkan pengotor yang masih terjebak dalam endapan dan tidak hilang saat penambahan etanol yang pertama. Endapan yang dihasilkan disaring kemudian dikeringkan dalam oven. Massa endapan yang diperoleh yaitu 1,8667 gram dengan rendemen sebesar 61,6%.
Pada pembuatan isomer trans-kalium dioksalatodiakuo kromat (III) ketika penambahan asam oksalat akan menyebabkan adanya efek trans pada senyawa kompleks. Pada reaksi ini terjadi penggantian 4 ligan monodentate aquo oleh ligan bidentat oksalato. Hal ini terjadi karena ligan bidentat oksalato memiliki kekuatan efek trans lebih besar daripada ligan monodentate aquo, ligan aquo tersebut menjadi labil, sehingga mudah digantikan oleh ligan oksalato (Keenan, 1991).
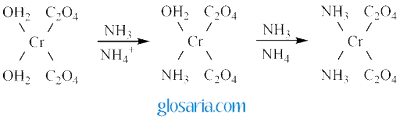
Uji kemurnian kristal dilakukan untuk membedakan yang mana isomer trans-kalium dioksalatodiakuo kromat (III) dan isomer cisnya. Kristal komples yang diperoleh dari percobaan diletakkan pada kertas saring. Lalu dilakukan penetesan amonia encer. Pada saat ditambahkan NH3 ke dalam kompleks cis-kalium dioksalatodiakuo kromat (III) padatan larut dan menyebar pada kertas saring dan warnanya hijau tua. Senyawa ini memiliki kelarutan lebih tinggi dan pada isomer trans, sehingga kristal cepat larut dengan penetesan air. Warna hijau tua merupakan warna dari senyawa kompleks cis-diammindioksalato kromat (III). Ligan H2O dapat digantikan oleh ligan NH3 karena ligan H2O pada posisi cis memiliki daya tolakan yang besar sehingga mudah digantikan oleh NH3. Reaksi kompleks cis-kalium dioksalatodiakuo kromat (III) dengan NH3 sebagai berikut:
(Keenan, 1991)
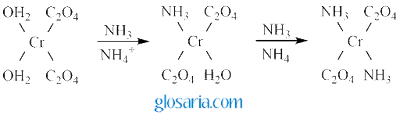
Pada saat ditambahkan NH3 ke dalam kompleks trans-kalium dioksalatodiakuo kromat (III) akan berwarna cokelat dan tidak menyebar yang merupakan senyawa kompleks dari trans-diammin dioksalato kromat (III). Reaksi kompleks trans-kalium dioksalatodiakuo kromat (III) dengan NH3 sebagai berikut:
(Keenan, 1991)
Senyawa trans yang terbentuk sangat sedikit. Hal ini dikarenakan pada percobaan ini terdapat akuades yang berlebihan. Akuades merupakan ligan yang memiliki efek trans yang buruk, sehingga dengan banyaknya akuades yang terdapat dalam larutan semakin sulit untuk membentuk isomer trans.
G. Kesimpulan
Berdasarkan percobaan yang telah dilakukan dapat disimpulkan bahwa:
- Senyawa kompleks cis dan trans dari garam kompleks kalium dioksalatodiakuo kromat (III) dapat disintesis dengan mencampurkan kalium dikromat dan asam oksalat dihidrat dengan perlakuan berbeda. Isomer cis-kalium dioksalatodiakuo kromat (III) memiliki massa 1,8667 gram dengan rendemen 61,6%. Isomer trans-kalium dioksalatodiakuo kromat (III) memiliki massa 0,0104 gram dengan rendemen 0,34%.
- Pada uji kemurnian, isomer cis berwarna hijau tua dan cepat menyebar pada kertas saring. Sedangkan isomer trans berwarna coklat dan tidak menyebar pada kertas saring.
H. Daftar Pustaka
- Achnadi, S. 1987. General Chemistry. Bogor: PT. Gelora Aksara Pratama.
- Arsyad. 2002. Kamus Kimia Arti dan Penjelasan Istilah. Jakarta: Gramedia.
- Cahyono. 1991. Segi Praktisi dan Metode Pemisahan Senyawa Organik. Semarang: Universitas Diponegoro.
- Cotton, F. A. dan Wilkinson, G. 1989. Kimia Anorganik Dasar. Jakarta: UI Press.
- Day, M. C. Jr. dan J. Selbian. 1987. Kimia Anorganik Teori. Yogyakarta: UGM Press.
- Harjadi. 1990. Ilmu Kimia Analitik Dasar. Jakarta: Gramedia.
- Keenan. 1991. Ilmu Kimia Untuk Universitas. Jakarta: Erlangga.
- Saito, T. 1996. Buku Teks Online Kimia Anorganik. Tokyo: Shotten.
- Sukardjo. 1992. Kimia Anorganik. Yogyakarta: Bina Aksara.
- Sumo, U. F. 1992. Pengantar Kimia Organik. Jakarta: PT. Gramdia Pustaka Utama.
- Shriver, D. F. 1940. Inorganic Chemistry. New York: W. H. Freeman and Company.

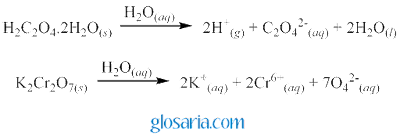
Posting Komentar untuk "Laporan Praktikum Sintesis Senyawa Kompleks Cis dan Trans Kalium Diakuodioksalato Kromat (III)"