Penggolongan Unsur Kimia
Unsur Kimia
Semua zat dialam ini tersusun atas unsur-unsur. Apa yang dimaksud dengan unsur kimia? Unsur adalah zat yang paling sederhana dan tidak dapat dibagi/diurai lagi menjadi zat yang lebih sederhana melalui cara-cara kimia biasa.Unsur-unsur didapatkan dalam berbagai wujud yang dapat berupa atom, ion, ataupun senyawa. Suatu unsur dapat memiliki beberapa isotop dengan nomor atom yang sama. Sifat fisis dan sifat kimia unsur-unsur kimia dipelajari dalam salah satu cabang ilmu kimia, yaitu cabang ilmu kimia unsur.
Menurut beberapa referensi sampai tahun 2011, terdapat sekitar 118 unsur yang telah dikenali. Rinciannya adalah 98 unsur merupakan unsur yang ditemukan secara alami, sedangkan 20 unsur lainnya merupakan unsur yang disintesis di laboratorium. Contoh unsur antara lain: Fe (Ferrum) besi, Au (Aurum) emas, At (Astatin) astatin, O (Oksigen).
Penggolongan Unsur-Unsur Kimia
Unsur-unsur yang terdapat secara alami di alam disebut sebagi unsur alami, sedangkan unsur-unsur yang dibuat oleh ilmuwan disebut sebagai unsur buatan.Umumnya unsur-unsur yang ditemukan di alam berada dalam bentuk persenyawaan seperti natrium dalam garam dapur. Tembaga, perak, platina dan emas merupakan contoh unsur yang terdapat bebas di alam yang tidak dalam bentuk persenyawaan.
Pada mulanya unsur dikelompokkan berdasarkan unsur logam dan unsur non-logam. Saat ini unsur telah dikelompokkan secara sistematis dalam bentuk Tabel Periodik Unsur atau dikenal juga Sistem Periodik unsur (SPU).
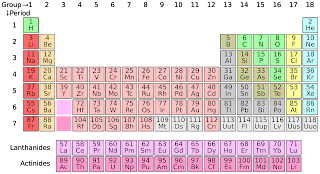 |
| Tabel Periodik Unsur (pixabay) |
Tabel Periodik Unsur
Di dalam tabel periodik unsur, unsur-unsur kimia diklasifikasikan ke dalam beberapa golongan dan periode. Setiap golongan unsur dalam tabel periodik memiliki nama-nama khas sesuai unsur yang menempati golongan tersebut, seperti pada unsur golongan 1A yang disebut dengan golongan alkali.Pengelompokkan ini didasarkan atas kemiripan sifat, baik sifat atom dan senyawanya. Pelambangan unsur-unsur dilakukan dengan menggunakan lambang-lambang abjad yang mewakili nama-nama unsur tersebut. Huruf pertama lambang unsur selalu huruf kapital, sedangkan huruf kedua biasanya dengan huruf bukan kapital.
Penggolongan unsur menurut jenis subkulit yang terisi digolongkan menjadi golongan unsur utama, gas mulia, unsur transisi (logam transisi), lantanida, dan aktinida.
Unsur golongan utama terdiri dari unsur-unsur golongan 1A hingga 7A. Gas mulia merupakan unsur golongan 8A. Logam transisi merupakan unsur-unsur golongan 1B, 3B sampai 8B.
Berdasarkan komposisi orbitalnya, unsur-unsur diklasifikasikan menjadi golongan unsur blok s, blok p, blok d, dan blok f.
Blok s terdiri dari unsur-unsur golongan 1 dan 2, blok p terdiri dari unsur-unsur golongan 13 sampai 16, blok d terdiri dari unsur-unsur golongan 3 samapi 12, dan blok f terdiri dari unsur-unsur golongan lantanida (lantanoid) dan aktinida (aktinoid).
Menurut teori yang masih diterima sampai saat ini, unsur yang pertama kali terbentuk adalah hidrogen dan helium. Hidrogen dan helium terbentuk sesaat setelah big bang. Di alam, kelimpahan unsur hidrogen dan helium merupakan yang paling besar.
Unsur-unsur Membentuk Senyawa
Suatu unsur dapat bereaksi dengan satu atau lebih unsur lainnya membentuk senyawa. Suatu unsur dapat berikatan dengan unsur yang lain membentuk senyawa. Misal air(H2O), Natrium Klorida (NaCl), Karbondioksida (CO2) dan lain sebagainya.Menurut teori yang masih diterima sampai saat ini, unsur yang pertama kali terbentuk adalah hidrogen dan helium. Hidrogen dan helium terbentuk sesaat setelah big bang. Di alam, kelimpahan unsur hidrogen dan helium merupakan yang paling besar.
Sumber referensi:
Chang, Raymond. 2004. Kimia Dasar: Konsep-konsep inti jilid 1, edisi ketiga. Jakarta: Penerbit Erlangga
Saito, Taro. 1996. Kimia Anorganik. Iwanami Publishing Company
Saito, Taro. 1996. Kimia Anorganik. Iwanami Publishing Company
Posting Komentar untuk "Penggolongan Unsur Kimia"