Korosi: Pengertian, Proses, Faktor Penyebab, dan Cara Pencegahan Korosi
Korosi merupakan peristiwa rusaknya logam atau yang juga sering disebut dengan pengkaratan. Faktor-faktor penyebab korosi antara lain: air, elektrolit, permukaan logam dan sebagainya. Terdapat beberapa cara pencegahan korosi seperti pelapisan dengan senyawa tahan karat, pembungkusan, dan sebagainya.
Pengertian Korosi
Korosi adalah kerusakan yang terjadi pada benda-benda logam yang diakibatkan oleh pengaruh lingkungan. Besi merupakan logam yang mengalami korosi atau perkaratan. Pengaruh lingkungan yang menyebabkan logam seperti besi mengalami korosi antara lain senyawa asam, air, dan perubahan suhu dalam jangka waktu yang cukup lama.
Proses Terjadinya Korosi
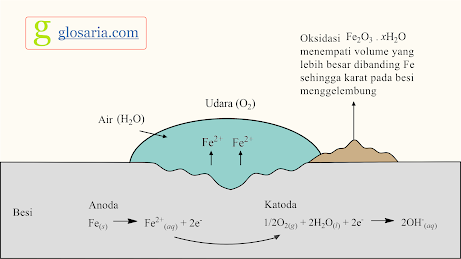
Proses korosi pada perkaratan besi dapat dijelaskan secara elektrokimia. Elektrokimia merupakan proses terjadinya reaksi reduksi oksidasi (redoks). Korosi dapat terjadi pada proses perkaratan besi yang membentuk oksidasi besi (Fe2O3.nH2O). Pada proses perkaratan besi, logam besi akan tereduksi oleh oksigen yang berasal dari udara. Berikut ini adalah reaksi korosi pada besi:
Ion Fe2+ tersebut kemudian mengalami oksidasi lebih lanjut dengan reaksi:
Berdasarkan reaksi yang terjadi, nilai potensial reaksi yang dihasilkan adalah Eoreaksi > 0 (positif). Hal ini membuat besi mudah mengalami korosi. Logam dengan nilai potensial elektrode lebih besar dari 0,4 V akan sulit mengalami korosi karena akan menghasilkan Eoreaksi < 0 (negatif). Contohnya seperti perak, platina, dan emas sulit mengalami korosi karena memiliki nilai potensial elektrode lebih besar dari 0,4 V.
Faktor Penyebab Korosi
Adapun korosi dapat terjadi disebabkan oleh faktor-faktor berikut ini:
1. Air dan kelembapan udara
Salah satu faktor penting berlangsungnya korosi yaitu air dan kelembapan udara. Suatu logam akan mudah mengalami korosi jika berada pada lingkungan dengan udara lembap (mengandung banyak uap air). Berbeda halnya jika logam ditempatkan pada lingkungan dengan kadar uap air yang rendah seperti gurun makan logam tersebut akan sulit mengalami korosi.
2. Elektrolit
Elektrolit (asam atau garam) merupakan media untuk terjadinya transfer muatan. Hal tersebut memudahkan oksigen di udara untuk mengikat elektron. Air hujan yang mengandung asam serta air laut yang mengandung garam merupakan media yang dapat mempercepat terjadinya korosi.
3. Permukaan logam yang tidak rata
Logam dengan permukaan yang tidak rata memudahkan terjadinya korosi. Penyebabnya adalah terbentuknya kutub-kutub muatan yang berperan sebagai anoda dan katoda. Berbeda dengan logam yang permukaannya licin dan bersih, maka akan sukar terjadi korosi. Hal tersebut disebabkan sulit terbentuknya kutub-kutub muatan yang berperan sebagai anoda dan katoda.
4. Terbentuknya sel elektrokimia
Sel elektrokimia dapat terbentuk apabila dua logam yang berbeda potensial saling bersentuhan pada lingkungan berair atau lembap. Logam yang memiliki potensial lebih rendah akan melepaskan elektron dan mengalami oksidasi ketika bersinggungan dengan logam yang potensialmya lebih tinggi. Oksidasi merupakan penyebab korosi lebih cepat terjadi pada logam dengan potensial rendah.
Cara Pencegahan Korosi
Peristiwa korosi pada logam sulit untuk dicegah, namun dapat dihambat dengan beberapa cara berikut:
- Pengecatan
- Penggunaan pelumas
- Pembalutan dengan plastik
- Galvanisasi
- Penyepuhan
- Sacrifical Protection
Penjelasan secara lengkap beberapa cara mencegah korosi dapat Anda baca pada artikel 7 Cara Pencegahan Korosi Pada Besi

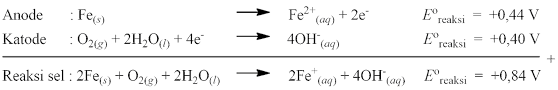
Posting Komentar untuk "Korosi: Pengertian, Proses, Faktor Penyebab, dan Cara Pencegahan Korosi"